www.khayma.com/fatsvt
تمييز الجسم بين ما هو ذاتي و غير ذاتي
المناعة غير النوعية أو الطبيعية
المناعة النوعية
الاستجابة المناعية النوعية ذات وسيط خلطي
الاستجابة المناعية النوعية ذات وسيط خلوي
اضطرابات الاستجابة المناعية
بعض وسائل تدعيم الاستجابات المناعية
متحركات الاستجابة المناعية
تمييز الجسم بين ما هو ذاتي وغير ذاتي
يهتم علم المناعة بدراسة كل الآليات التي تمكن الجسم من الحفاظ على تماميته أي تمييز كل ما هو ذاتي والحفاظ عليه وغير الذاتي للتخلص منه.
فكيف يمكن للجسم التمييز بين الذاتي وغير الذاتي؟
ما هي آليات دفاع الجسم ضد غير الذاتي؟
ما هي اضطرابات الجهاز المناعتي؟
كيف يمكن تدعيم الاستجابة المناعية؟
I / تمييز الجسم بين ما هو ذاتي وغير ذاتي
1- معطيات تجريبية وسريرية:
للكشف عن العامل المحدد للذاتي، نقترح دراسة النتائج التجريبية والسريرية الممثلة في الوثيقتين1 و2 .
تبين الوثيقة 1 نتائج تجارب التطعيم الجلدي بين سلالات من الفئران، بينما تمثل الوثيقة2 ملاحظات سريرية لتطعيم جلدي بين أفراد ذوي قرابة مختلفة.
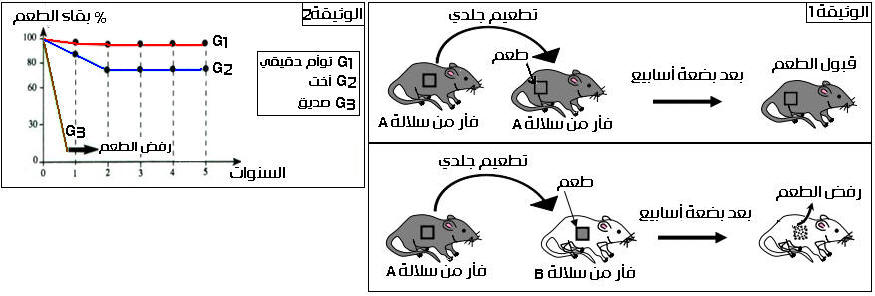
1 ـ باستغلالك للوثيقة1، فسر النتائج المحصل عليها.
2 ـ اعتمادا على الوثيقة2، استخلص العامل المحدد للذاتي.
3 ـ انطلاقا من المعطيات السابقة، استنتج العلاقة التي تربط جهاز المناعة بكل من الذاتي وغير الذاتي.
الإجابة
2 ـ تركيب بروتينات CMH
أدت الأبحاث إلى اكتشاف بروتينات توجد على الغشاء السيتوبلازمي للخلايا المنواة تتدخل في تحديد ما هو ذاتي ( واسمات الذاتي)، سميت نظام HLA(Human Leucocyte Antigen لأنها اكتشفت أول مرة فوق غشاء الكريات البيضاء، وتمت ملاحظتها أيضا فوق غشاء الخلايا المنواة وسميت بذلك المركب الرئيسي للتلاؤم النسيجي CMH( Complexe Majeur d’Histocompatibilité
يتحكم في تركيب بروتينات CMH أربع مورثات محمولة على الصبغي 6 وهي المورثات A ,C,B,D. تتميز بالخاصيات التالية:
- هي مورثات مرتبطة أي محمولة على نفس الصبغي.
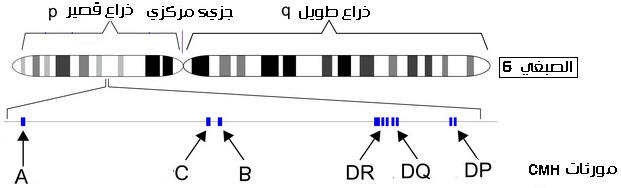
Philip Deitiker, Wikimedia Commons
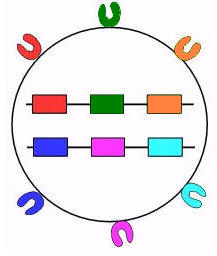
- متعددة الحليلات أي لكل مورثة عدة حليلات (في كل مرة تكتشف حليلات جديدة). انظر الرابط
مثال: نمط وراثي لشخص معين
انظر الرابط
- الحليلات متساوية السيادية.
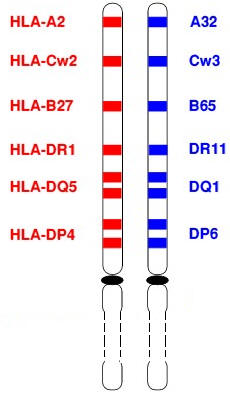
تمثل الوثيقة التالية جزء من النمط الوراثي لـ CMH عند زوجين.
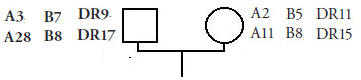
1 ـ استنادا إلى الوثيقة، حدد التوافقات الممكنة CMH لخلف الزوجين ( في غياب العبور الصبغي).
2 ـ اعتمادا على مقارنة الأنماط الوراثية للأبوين وخلفهما، بين أي الأبناء أكثر توافقا مع الأم فيما يخص CMH .
الإجابة
3 ـ أصناف بروتينات CMH
يوجد صنفان رئيسيان من بروتينات CMH هما :
ـ بروتينات CMHI: توجد على سطح خلايا الجسم المنواة، يتحكم في تركيب هذا النوع المورثات B ، A و C. تتكون هذه البروتينات من سلسلتين بيبتيديتين α و β2m. (تتحكم في السلسلة β2m مورثة توجد على الصبغي15)
ـ بروتينات CMHII: توجد على سطح بعض الخلايا المناعية كاللمفاويات والبلعميات، تتحكم في تركيبها المورثة D. تتكون هذه البروتينات من سلسلتين بيبتيديتين α و β.
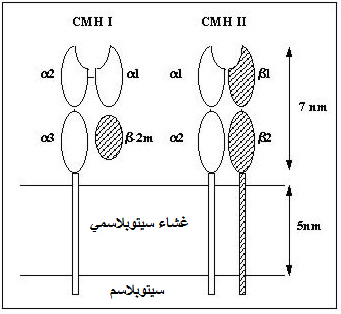
http://www2.vet-lyon.fr
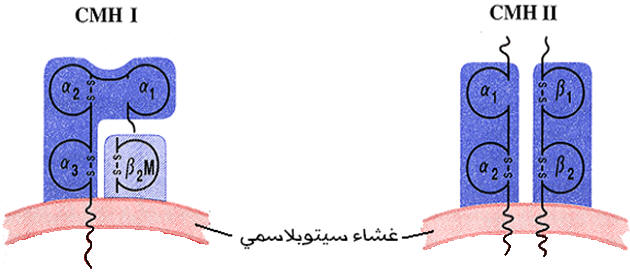
4 ـ دور بروتينات CMH :
في جميع الخلايا تجزئ أنزيمات خاصة عينة من البروتينات الموجودة في السيتوبلاسم إلى بيبتيدات، يرتبط كل بيبتيد بجزيئة CMH ويهاجر المركب بيبتيد ـ CMH إلى سطح الخلية، وهكذا تعرض الخلايا باستمرار محتواها البيبتيدي مما يمكن من حراسة مناعية:
ـ إذا كانت البيبتيدات المعروضة منحدرة من بروتينات عادية للخلية، فانه لا يحدث ارتباط بين الخلية والخلايا المناعية، وبالتالي غياب الاستجابة المناعية .انظر الوثيقة
ـ إذا كانت البيبتيدات المعروضة منحدرة من بروتينات غير عادية للخلية(بروتين شاذ لخلية سرطانية أو بروتين فيروسي) فانه يحدث ارتباط بين الخلية والخلايا المناعية، وبالتالي حدوث الاستجابة المناعية .انظر الوثيقة
هكذا يتبين أن مركب CMH هو مجموع المورثات المسؤولة عن تركيب بروتينات CMH المسؤولة عن تحديد الذاتي، ففي حالة زرع الأعضاء إذا كان CMH المعطي يخالف CMH المتلقي تحدث استجابة مناعتية مسؤولة عن رفض الطعم لذلك تسمى بروتينات CMH مولدات مضاد التلاؤم النسيجي.
II ـ الواسمات الثانوية للذاتي:
الكريات الحمراء خلايا بدون نواة وبالتالي لا يمكن إعتبار CMH مصدر تحديد الفصيلة الدموية(CMH جزيئات خاصة بالخلايا المنواة)
تحديد الفصيلة النسيجية يخضع لنظامين أساسيين (هناك أنظمة أخرى ثانوية) وهما نظام ABO ونظام Rhésus
1 ـ نظام ABO :
مرتبط بمورثة تتميز ب 3 حليلات وهي:
- الحليل A: يرمز إلى غليكوبروتينات غشائية تمثل مولدات مضاد غشائية ( تميز غشاء الكريات الحمراء صنف A).تسمى ايضا مولدات اللكد
- الحليل B: يرمز إلى غليكوبروتينات غشائية تمثل مولدات مضاد غشائية ( تميز غشاء الكريات الحمراء صنف B).
- الحليل O: يرمز إلى غليكوبروتينات غشائية غير محدثة لإستجابة مناعتية (الفصيلة O).
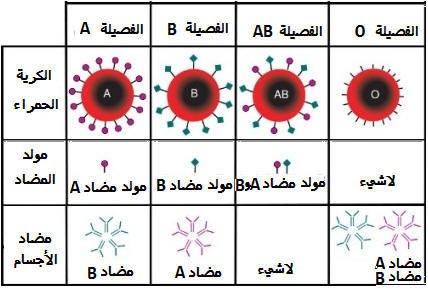
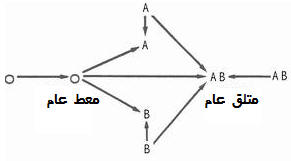
الحليل O متنحي والحليلات A و B متساوية السيادة.
O AB B A المظهر الخارجي
O/O A/B
B/B أو B/O
A/A أو A/O النمط الوراثي
يمكن اعتبار هذه الغليكوبروتينات الغشائية مصدر تحديد الفصيلة الدموية, وبما أن نظام ABO ينتج عن مورثة واحدة بعدد محدود من الحليلات (عكس جزيئات CMH) فإن عدد الفصائل الدموية قليل.
2 – نظام Rhésus :
إضافة إلى مولدات اللكد الناتجة عن نشاط المورثة المحددة للنظام ABO, هناك نوع أخر من مولدات المضاد قد يوجد على مستوى الكريات الحمراء وتسبب التلكد.
هذه الجزيئات تنتج عن نظام وراثي مستقل عن النظام السابق، مورثة تتميز بحليلين:
- الحليل Rh+ يرمز إلى مولد مضاد غشائي مسؤول عن تسييب إستجابة مناعتية.
- الحليل Rh- غياب مولد مضاد.
الحليل Rh+ سائد والحليل Rh- متنحي.
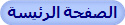
III ـ عناصر غير الذاتي
مجموع العناصر التي إذا دخلت الجسم تؤدي إلى رد فعل مناعي.
ـ يمكن أن يكون غير الذاتي خارجي المصدر:
- الجراثيم: البكتيريات، الحمات، الفطريات والحيوانات الأولية.
- الأعضاء والأنسجة الأجنبية عن الجسم.
ـ يمكن أن تكون عناصر ذاتية خضعت لتغير فاعتبرت غير ذاتية:
- خلايا الجسم الشاذة: الخلايا المسنة أو السرطانية.
www.khayma.com/fatsvt



 مقالة مفصلة:
مقالة مفصلة: 
 → 1 − p = 1 R 0 , {\displaystyle 1-p={\frac {1}{R_{0}}},}
→ 1 − p = 1 R 0 , {\displaystyle 1-p={\frac {1}{R_{0}}},}  → p c = 1 − 1 R 0 . {\displaystyle p_{c}=1-{\frac {1}{R_{0}}}.}
→ p c = 1 − 1 R 0 . {\displaystyle p_{c}=1-{\frac {1}{R_{0}}}.} 



